|
На первую страницу | «Очерки научной жизни»: оглавление и тексты | Аннотация «Очерков» и об авторе | Отдельные очерки, выступления | Научно-популярные статьи (ссылки) | Список публикаций | Гостевая |
БИОХИМИЯ Т. 28, вып. 4, 1963 г. С. 625–634
Переход к английскому тексту (варианту) статьи
Г. И. АБЕЛЕВ, С. Д. ПЕРОВА, И. И. ХРАМКОВА, 3. А. ПОСТНИКОВА и И. С. ИРЛИН
Институт эпидемиологии и микробиологии им. Н. Ф. Гамалеи
Академии медицинских наук СССР, Москва
Проблема регуляции синтеза белка в клетке становится в настоящее время все более актуальной, особенно в связи с успехами в изучении адаптивного образования ферментов у бактерий.
Обнаружение специфических генетических механизмов у бактерий, контролирующих активность структурных генов [1; 2], поставило вопрос о наличии двойного генетического контроля белкового синтеза в клетках животных и о роли регулирующих механизмов в процессе дифференцировки и при малигнизации клеток [3–6]. В связи с этим приобретает особый интерес выявление и изучение таких белков, синтез которых резко активируется или подавляется в онтогенезе или при малигнизации ткани.
В настоящей работе обнаружен сывороточный α-глобулин, активно синтезируемый мышиным эмбрионом, но отсутствующий в крови и органах взрослых мышей. Показано также, что активный синтез этого α-глобулина происходит в клетках перевиваемого рака печени и, по-видимому, в регенерирующей печени мышей. Можно думать, что изучение условий образования этого белка окажется полезным для понимания процессов репрессии и активации белкового синтеза в клетках животных и роли этих явлений при малигнизации. Выявление и изучение эмбрионального α-глобулина проводили иммунохимическими методами, что позволило выявить этот белок в многокомпонентных системах и проследить его судьбу в различных экспериментальных условиях.
В работе использовали сыворотки мышиных эмбрионов второй половины беременности, сыворотки мышей, взятых в разные сроки после рождения, а также мышей с различными опухолями. Кровь брали после перерезки подключичного сосудистого пучка, обрабатывали по обычной методике и хранили на холоду с мертиолатом (1 : 10 000). Работу проводили в основном на мышах линии СЗНА. Были использованы также линии C57BL, СЗН, CC57W, СС57Вг и беспородные животные.
Большая часть опытов была поставлена на гепатоме штамма XXIIа. Первоначально эта опухоль была индуцирована в 1951 г. у мышей СЗНА при помощи ортоаминоазотолуола [7] и с тех пор пассируется на мышах той же линии. Опухоль обладает высокой скоростью роста, развивается на 6–7 день после прививки и перевивается на 13–14-й день. Гепатомы 22, 38 и 46 – медленно растущие опухоли того же происхождения, что и ХХIIа, микроскопически состоят из клеток, напоминающих печеночные. Характеристика гепатом приведена ранее [7–9].
Были использованы две кроличьи антисыворотки против сыворотки новорожденных мышей (анти-НМ), две против сыворотки взрослых мышей (анти-ВМ) и антисыворотки к гепатоме ХХIIа. Сыворотки анти-НМ и анти-ВМ получали по следующей схеме иммунизации: первая инъекция под кожу – 3 мл сыворотки с дополнителем Фрейнда и антибиотиками; вторая и третья инъекции – без дополнителя Фрейнда, по 3 мл сыворотки подкожно с интервалами в 14 и 7 дней. Кровь брали через 7 и 14 дней после последней инъекции. Антигепатомные сыворотки получали по схеме, описанной ранее (9].
Истощение сывороток анти-НМ проводили путем добавления к ним равного объема сыворотки взрослых мышей с последующей инкубацией при 37° в течение 1 часа, а затем при 4° 16–18 час. Выпавший осадок удаляли путем центрифугирования при 10 000 об/мин (20–30 мин.). Надосадочная жидкость содержала антитела только к специфическим антигенам эмбриональной сыворотки.
Определение антигенов проводили методом преципитации в агаре в микромодификации [10] и иммуноэлектрофореза в полумикромодификации [11; 12]. В части опытов использовали метод высоковольтного микроэлектрофореза по Виему [13].
Выделение α-глобулина из сыворотки новорожденных мышей производили методом препаративного зонального электрофореза в агаре. Обрабатывали по 2 мл сыворотки. Разделение вели в блоке 1%-ного агара на веронал-мединаловом буфере, рН 8,6, μ 0,025; размер блока 11х15х1 см. Время разделения 6 час. при градиенте потенциала 4–4,5 в/см и силе тока 80 ма. Зона изучаемого антигена располагалась между местом внесения препарата и альбумином. Элюцию белков проводили при отжимании оттаивающего агара в центрифуге. Аппарат для препаративного электрофореза и методика опытов детально описаны ранее [12].
Окончательную очистку антигена, полученного при электрофорезе сывороток, осуществляли методом иммунофильтрации [11], разработанным для выделения того же антигена из экстракта гепатомы ХХIIа. При очистке специфического α-глобулина из сывороток новорожденных мышей и из сывороток мышей с гепатомой в качестве «фильтра» использовали сыворотки анти-ВМ. α-Глобулин из экстракта гепатомы выделяли описанным ранее методом иммунофильтрации [11] с той разницей, что антиген из агара извлекали методом вымораживания [12].
Гетеротрансплантации гепатомы ХХIIа проводили на крысах и хомяках по методике, рекомендованной Васильевым [14]. Трех-, четырехнедельным крысам одновременно с прививкой гепатомы вводили кортизон (Corton-Acetate, Merk) в дозе 2,5 мг каждой. Повторные введения кортизона производили через каждые 3 дня после прививки опухоли. Опухолевые узелки прощупывались на 7–8-й день после прививки и достигали максимальной величины на 10–13-й день.
Хомякам опухоль прививали в защечный мешок одновременно с введением кортизона (2,5 мг на животное). Введение кортизона повторяли с интервалами в 3 дня. Опухолевые узелки появлялись у единичных животных в среднем через 2 недели после прививки и по размерам не превышали горошину (0,06–0,08 ).
Гепатому ХХIIа культивировали in vitro следующим образом. Клеточную суспензию ткани гепатомы ХХIIа, полученную после пипетирования мелкоизмельченных кусочков опухоли в среде № 199 с 10% телячьей сыворотки, промывали двухкратным центрифугированием (800 об/мин; 5 мин.). Осадок разводили средой № 199 с 30% телячьей сыворотки (ростовая среда) до конечной концентрации 1 млн. живых клеток в 1 мл. Количество живых клеток определяли по стандартной методике окрашиванием трипановым синим [15]. Клеточную взвесь разливали по флаконам и через 18 час. неосевшие клетки удаляли. Смену среды производили через 3–4 дня. Монослой, состоящий из темных округлых или полигональных клеток с небольшим количеством фибробластов, образовывался в 1–2-ю неделю культивирования. По мере культивирования количество фибробластов увеличивалось, и к концу 4-й недели соединительнотканные элементы почти полностью замещали клетки гепатомы.
Специфический компонент эмбриональной сыворотки мышей наиболее просто выявлялся при помощи сывороток анти-НМ, истощенных сыворотками нормальных взрослых мышей. Этот компонент четко реагировал как в реакции преципитации в агаре, так и при иммуноэлектрофорезе.
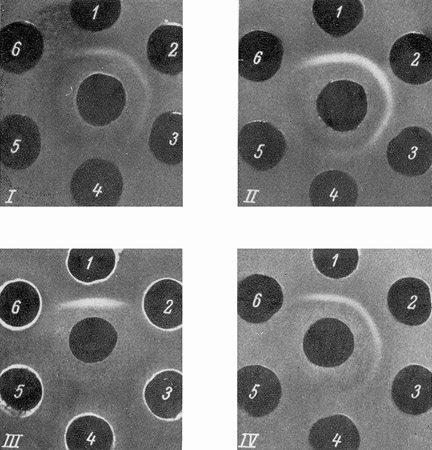
Определение эмбрионального компонента в сыворотках мышей реакцией преципитации в агаре. Анти-НМ-сыворотки, истощенные равным объемом сывороток взрослых мышей, не реагировали с последними, но давали полосу преципитации с сыворотками новорожденных мышей в разведениях до 1/1000–1/2000. Для проведения количественных определений антигена и для повышения чувствительности реакции мы пользовались методом титрования со стандартной тест-системой [12; 16]. Для этого в центральную лунку (рис. 1) заливали истощенную анти-НМ-сыворотку, а в верхнюю – сыворотку новорожденных мышей, взятую в оптимальном разведении, при котором реагирующие антиген и антитело находятся в зоне эквивалентности или вблизи от нее и образуют наиболее четкую линию преципитации.

| Рис. 1. Титрование сывороток мышей – новорожденных, однонедельных, взрослых и привитых гепатомой ХХIIа |
| В центральных лунках – истощенная анти-НМ-сыворотка: 1 – антиген тест-системы (I) 2–6 – разведения сыворотки новорожденных от 1/512 до 1/8200; (II) 2–6 – разведения сыворотки однонедельных мышей от 1/128 до 1/2048; (III) 2–6 – разведения сыворотки взрослой мыши от исходной до 1–1/16; (IV) 2–6 – разведения сыворотки мышей с гепатомой ХХIIа от 1/128 до 1/2048 |
При сравнении тест-системы с различными разведениями исследуемых образцов можно было, во-первых, видеть, что определяемый в них антиген идентичен антигену тест-системы и, во-вторых, выявлять подпороговые концентрации антигена, которые не образуют сами полосу преципитации, но влияют на форму преципитата тест-системы [12; 16]. На рис. 1 представлены результаты титрования сывороток мышей, взятых на разных стадиях онтогенеза и мышей с гепатомой при помощи стандартной тест-системы.
В табл. 1 приведены данные о содержании антигена в сыворотках эмбриона второй половины беременности, а также в сыворотках мышей в разные сроки после рождения и мышей, привитых гепатомой XXIIа. Все данные были получены при помощи одной и той же стандартной тест-системы. Концентрацию антигена определяли по конечному разведению испытуемого препарата, дававшему реакцию с тест-системой. Титр антигена в сыворотке эмбриона, реагировавшей вплоть до разведения 1 : 4000, был принят за 100%; по отношению к нему пересчитывали величины, найденные в других сыворотках. Предел чувствительности метода составлял 0,025%. Из данных, приведенных в табл. 1, видно, что антиген в наибольшей концентрации присутствовал в сыворотке эмбриона и новорожденных мышей и что в течение первых недель после рождения уровень антигена снижался ниже порога чувствительности реакции, т. е. по крайней мере в 4000 раз. Антиген вновь появлялся в сыворотках мышей, привитых гепатомой XXIIа.
| Эмбрионы | Ново- рожденные | Недели после рождения | Мыши с гепатомой | ||||
| I | II | III | IV | V | |||
| 100 | 50 | 25 | 0,75 | – | – | – | 6 |
Следует отметить, что относительная концентрация антигена в сыворотках беременных мышей была ~ 0,25%. Следовательно, некоторая часть антигена переходит через плаценту в кровь матери.
Иммуноэлектрофоретическая характеристика специфического компонента эмбриональной сыворотки. На рис. 2, А приведен результат иммуноэлектрофоретическото анализа сыворотки новорожденной мыши. Истощенная анти-НМ-сыворотка четко выявляла антиген в зоне α-глобулинов. На иммунофореграмме, проявленной нативной анти-НМ-сывороткой, видно, что этот антиген являлся преобладающим компонентом в α-глобулиновой фракции.
В сыворотке новорожденных мышей после проявления истощенной анти-НМ-сывороткой обнаруживался еще один антиген, расположенный вблизи места нанесения препарата (рис. 2, А). Концентрация этого антигена была значительно ниже, чем α-глобулина с более высокой подвижностью, и при использованных соотношениях антигена и антител в тест-системе полоса этого антигена не проявлялась. Чтобы определить, какой белковой фракции сыворотки соответствует эмбриональный α-глобулин, в строго идентичных условиях проводили электрофорез сыворотки новорожденных и очищенного антигена (см. ниже), после этого очищенный антиген выявляли при помощи анти-НМ-сыворотки. При совмещении электрофореграммы и иммуноэлектрофореграммы дуга преципитации очищенного антигена точно совпадала с зоной α-глобулина сыворотки новорожденных (рис. 2, Б).
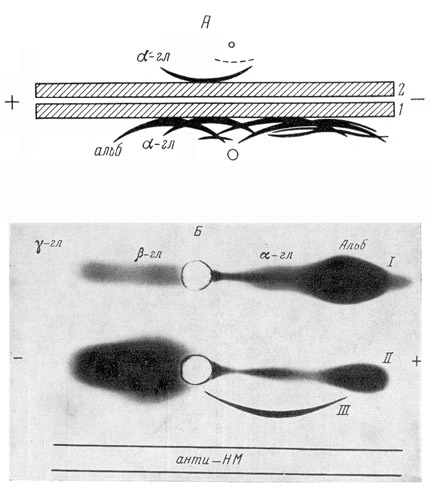
| Рис. 2. Иммуноэлектрофоретическая характеристика эмбрионального α-глобулина |
| А – иммуноэлектрофорез сыворотки новорожденных мышей. Проявлено: 1 – анти-НМ-сывороткой; 2 – истощенной анти-НМ-сывороткой. Б – совмещенные электрофореграммы сыворотки новорожденных мышей (II) и иммуноэлектрофореграммы очищенного эмбрионального α-глобулина (III), проявленного анти-НМ-сывороткой. I – электрофореграмма сыворотки взрослых мышей |
Для дальнейшей характеристики эмбрионального α-глобулина проводили его выделение из сыворотки новорожденных мышей, мышей с гепатомой XXIIа и из экстракта гепатомы XXIIа. α-Глобулин выделяли из сыворотки методом препаративного электрофореза в агаре с последующей очисткой методом иммунофильтрации.
Очищенный эмбриональный α-глобулин реагировал только с анти-НМ- и антигепатомными сыворотками и не взаимодействовал с анти-ВМ-сыворотками как в реакции преципитации в агаре (рис. 3, А), так и при иммуноэлектрофорезе (рис. 3, Б).
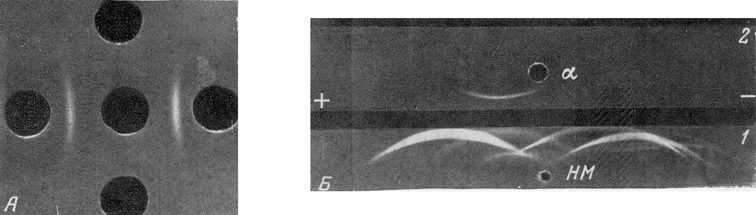
| Рис. 3. Характеристика очищенного эмбрионального α-глобулина |
| А – в центре очищенный α-глобулин; слева и справа анти-НМ, снизу и сверху анти-ВМ-сыворотки, Б – НМ-сыворотка новорожденной мыши; α – очищенный эмбриональный α-глобулин, 1 – анти-НМ-сыворотка; 2 – анти-ВМ-сыворотка |
Отсутствие антител к эмбриональному α-глобулину в анти-ВМ-сыворотках было показано также методом аналитической иммунофильтрации. В агаровой пластинке вырезали прямоугольный резервуар (рис. 4, А), в который заливали анти-ВМ-сыворотку, подвергнутую диализу против того же буфера, на котором был приготовлен агар. Рядом с резервуаром располагалась луночка, заполненная раствором пиронина, имеющего электрофоретическую подвижность в агаре, близкую к γ-глобулину кроличьей сыворотки [11]. При включении тока антитела сыворотки, находящиеся в ее γ-глобулиновой фракции, переносились электроосмотическим потоком к катоду и после 1,5 часа электрофореза занимали положение, указанное на рис. 4, А. На этом заканчивали первый этап электрофореза. Затем в агар в две симметрично расположенные лунки (рис. 4, Б) помещали α-глобулиновую фракцию сыворотки новорожденных мышей, содержащую примесь альбумина. Полюса переключали и проводили 2-часовой электрофорез, при котором происходило встречное движение антигенов сыворотки новорожденных к аноду, а антител анти-ВМ-сыворотки – к катоду. При встрече зон антигены, реагирующие с анти-ВМ-сывороткой, преципитировались, а антиген, не реагирующий с ней, проходил сквозь «фильтр» антител, не меняя своей подвижности. После проявления антисыворотками в «фильтрованном» образце определялся только специфический α-глобулин, в то время как в контрольном образце обнаруживалось еще 2 антигена.
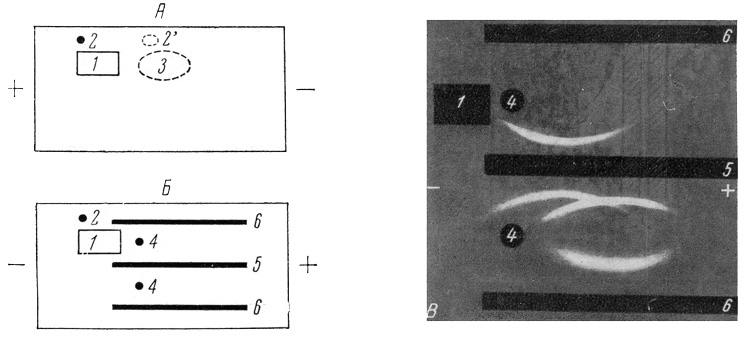
| Рис. 4. Аналитическая иммунофильтрация эмбрионального α-глобулина |
| А: 1 – резервуар для «фильтра»; 2 – лунка для пиронина; 2' – конечное положение пиронина; 3 – конечное положение γ-глобулина анти-ВМ-сыворотки. Б: 4 – лунки для внесения анализируемого антигена; 5 – траншея для анти-НМ-сыворотки, 6 – траншея для анти-ВМ-сыворотки. В – результат иммунофильтрации эмбрионального α-глобулина. Расположение реагентов как на рис. А и Б. Другие объяснения см. в тексте |
Таким образом, при помощи аналитической иммунофильтрации было показано, что в анти-ВМ-сыворотках не содержится обнаруживаемого количества антител к α-глобулину эмбриональной сыворотки.
Сравнение антигенов из сывороток новорожденных мышей и мышей с гепатомой. После прививки мышам гепатомы штамма XXIIа на 5–12-й день роста опухоли в сыворотке обнаруживали эмбриональный α-глобулин с высоким титром (до 1/256–1/512) (табл. 1). Тот же антиген обнаруживали и в экстракте опухоли, однако в меньшей концентрации, чем в сыворотке (титр 1/32–1/64).
Прежде всего необходимо было проверить, идентичен ли α-глобулин эмбриональной сыворотки компоненту, появляющемуся в сыворотке мышей с гепатомой. Для этого проводили сравнение специфических α-глобулинов, выделенных из сыворотки новорожденных мышей, мышей с гепатомой XXIIа и из экстракта этой опухоли.
Рис. 5 свидетельствует об идентичности трех антигенов, реагирующих как с анти-НМ, так и с противогепатомной антисывороткой. Все три антигена обладали также одинаковой электрофоретической подвижностью при иммуноэлектрофорезе в агаре.
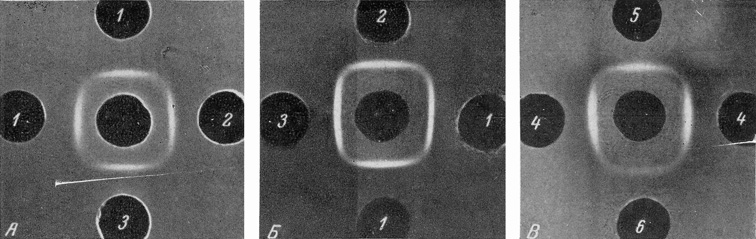
| Рис. 5. Сравнение эмбрионального α-глобулина различного происхождения |
| А – в центре анти-НМ-сыворотка; Б – в центре антигепатомная сыворотка; В – в центре истощенная анти-НМ-сыворотка. 1 – α-глобулин, выделенный из сыворотки новорожденных мышей; 2 – то же из экстракта гепатомы; 3 – то же из сыворотки мышей с гепатомой; 4 – экстракт гепатомы XXIIа, выросшей на мышах; 5 – сыворотка крыс, привитых гепатомой XXIIа; 6 – культуральная жидкость гепатомы XXIIа |
Таким образом, иммунологически и электрофоретически антигены не отличались и были идентичны эмбриональному сывороточному α-глобулину.
В связи с появлением в крови мышей, привитых гепатомой XXIIа, эмбрионального α-глобулина необходимо было решить вопрос о месте образования этого антигена. Образуется ли он в самой опухоли или возникает где-либо в другой ткани в ответ на прививку опухоли? Для ответа на этот вопрос были поставлены три серии опытов. В первой серии изучали наличие антигена у мышей, привитых другими опухолями, и у мышей с регенерирующей печенью; во второй – проводили гетеротрансплантацию мышиной гепатомы крысам с последующим определением мышиного эмбрионального α-глобулина и в третьей – изучали образование эмбрионального α-глобулина при культивировании гепатомы XXIIa in vitro.
Эмбриональный α-глобулин в сыворотках мышей с различными опухолями и мышей с регенерирующей печенью. Определение антигена проводили в сыворотках мышей, привитых медленнорастущими гепатомами штаммов XXII, XXXVIII и XLVI, а также с первичными и перевиваемыми опухолями различного происхождения, но не гепатомами. В эту группу входили следующие опухоли: карцинома Эрлиха, рак молочных желез (2 штамма), саркома Крокера, саркомы метилхолантреновые перевиваемые (4 штамма), саркомы бензантраценовые, перевиваемая и первичная, асцитная саркома I, перевиваемые лейкозы (5 штаммов), перевиваемый рак желудка, рак кожи (2 штамма). Сыворотку брали у мышей в различные сроки после прививки опухолей (7–92-й день), обычно, когда опухоли достигали больших размеров.
Одновременно изучали сыворотки мышей после частичной гепатэктомии*, через 24 часа после операции и через 48 час. во время максимального числа митозов в печени.
|
* Мыши с регенерирующей печенью были получены от д-ра В. И. Гельштейн, за что приносим ей глубокую благодарность. |
Для определений брали сыворотки самцов, чтобы исключить возможность попадания в изучаемую группу беременных животных, в сыворотках которых всегда имеется некоторое количество изучавшегося антигена. В каждой партии проводили определения у 2–10 особей. Данные определений приведены в табл. 2.
| Эмбрионы | Гепатэкто- мированные 24–48 час. | XXIIа | XXII | XXXVIII | XLVI |
| 100 | 0,1 – 0,2 | 6 | 0,1 – 0,2 | 0,2 – 0,4 | – |
| Карцинома Эрлиха | Саркома Крокера | Рак молочной железы, 2 штамма | Саркомы, 9 штаммов | Лейкозы, 5 штаммов | Рак желудка | Рак кожи, 2 штамма |
| – | – | – | – | – | – | – |
Приведенные данные показывают, что появление антигена в сыворотке имело место только при росте 3 из 4 штаммов гепатом и у мышей с регенерирующей печенью, причем максимальное накопление антигена наблюдалось при росте гепатомы XXIIа, обладавшей наибольшей скоростью роста. Значительно меньше антигена обнаруживалось в сыворотке мышей с гепатомами XXII, XXXVIII и после частичной гепатэктомии. При росте гепатомы XLVI и остальных опухолей другого происхождения антиген не обнаруживался. Следует отметить, что в экстрактах гепатом XXII, XXXVIII и в регенерирующей печени антиген, как правило, не мог быть выявлен. Наличие его было отмечено лишь в тех случаях, когда титр антигена в крови был выше, чем 1 : 8.
Таким образом, появление антигена в крови животных наблюдалось только после прививки им печеночных раков, а также при регенерации печени, т. е. в тех случаях, когда в организме животного имелись пролиферирующие клетки нормальной или малигнизированной печени.
Образование антигена в условиях гетеротрансплантации и культивирования in vitro. Опыты по гетеротрасплантации гепатомы XXIIа проводили на крысах и хомяках, обработанных кортизоном. На хомяках удачными были лишь единичные прививки: из 7 привитых животных опухоли развились только у 3 через 2 недели после прививки и достигали очень небольших размеров (0,06–0,08 г). В экстрактах этих опухолей при помощи стандартной тест-системы был обнаружен изучаемый антиген; при разведении экстрактов он не определялся. В крови привитых животных антиген не обнаруживался.
Более четкие результаты были получены при гетеротрансплантациях гепатомы XXIIа крысам, обработанным кортизоном. Опухоли развивались очень быстро, так же как у мышей, достигая на 10–13-й день максимальной величины (до 1,5 г). В сыворотке крыс с развивающимися опухолями и в экстрактах опухолей четко выявлялся эмбриональной мышиный α-глобулин, который давал реакцию идентичности с антигеном стандартной тест-системы (рис. 5, В) и имел ту же электрофоретическую подвижность, что и мышиный антиген. Результаты соответствующих опытов приведены в табл. 3. Из данных табл. 3 видно, что мышиный антиген появлялся в крови крыс на 5-й день развития опухоли, достигая максимальной концентрации на 6–12-й день, и в период рассасывания опухоли исчезал из сыворотки. Интересно отметить, что концентрация антигена в самой опухолевой ткани (с учетом степени разведения в экстракте) превышала его концентрацию в сыворотке на ранних стадиях развития опухоли. Антиген, выявляемый у крыс с мышиной гепатомой, был полностью идентичен мышиному α-глобулину. Однако у новорожденных крыс и у крыс, привитых асцитной крысиной гепатомой Зайдела, обнаруживался антиген, дающий перекрестные редакции с мышиным эмбриональным α-глобулином. Однако указанный крысиный антиген отсутствовал в сыворотках взрослых крыс; он не был идентичен мышиному антигену и достаточно четко отличался от него.
| Дни после прививки | III | V | VI | ||||||||
| Порядковый номер крысы | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| Вес опухоли, г | 0,58 | 0,25 | 0,54 | 0,52 | 0,42 | 0,55 | 0,46 | 0,5 | 0,62 | 0,54 | 0,42 |
| Титр антигена в сыворотке крыс | Исх. (±) | Исх. (±) | 1 : 2 | 1 : 2 | Исх. | 1 : 2 (±) | 1 : 2 | 1 : 8 (±) | 1 : 16 | 1 : 4 | |
| в экстракте
гепатомы (1/4) | Исх. | Исх. | 1 : 2 | 1 : 2 | 1 : 8 | 1 : 2 | 1 : 2 (±) | 1 : 4 (±) | 1 : 4 | 1 : 2 | 1 : 2 |
| Дни после прививки | IX | XI | XII | XIV | ||||||||
| Порядковый номер крысы | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 |
| Вес опухоли, г | 1,8 | 0,24 | 1,53 | 1,97 | 1,55 | 0,43 | 1,32 | 1 | 0,52 | 1,44 | 0,3 | 0,42 |
| Титр антигена в сыворотке крыс | 1 : 256 | 1 : 2 | 1 : 16 | 1 : 16 | 1 : 16 | – | 1 : 32 | – | – | 1 : 4 (±) | – | – |
| в экстракте гепатомы (1/4) | 1 : 64 | Исх. | 1 : 8 | 1 : 8 | 1 : 2 | Исх. | 1 : 32 (±) | 1 : 16 | Исх. (±) | 1 : 16 | – | – |
Примечание. Исх. – антиген определяли только в неразведенном образце;
1/2 и т.п. – антиген определяли при разведении образца 1/2 и т.п.; (±) – сомнительный результат; – – отрицательный результат.
Таким образом, опыты по гетеротрансплантации мышиной гепатомы крысам свидетельствуют об образовании антигена самой мышиной опухолью. Окончательное доказательство этого положения было получено в опытах по культивированию гепатомы XXIIa in vitro.
В этих опытах, чтобы исключить механическую примесь антигена при засеве клеток, перед сменой фазы проводили промывание растущей культуры определенным объемом среды, после чего в промывной и в культуральной жидкостях исследовали содержание антигена со стандартной тест-системой. Кроме того, культуральную жидкость, слитую после инкубации в ней культур, концентрировали в 7–8 раз, после чего также проводили определение антигена. В качестве контролей служила чистая ростовая среда, среда, сконцентрированная в 8–10 раз, и культуральные жидкости, полученные из культуры нормальных фибробластов и фибробластов хомяка, трансформированных вирусом полиомы. Данные соответствующих опытов приведены в табл. 4. Образование антигена наблюдалось в течение всего периода роста культуры гепатомы и прекращалось, когда гепатомные клетки замещались фибробластами. Ни в одном из контролей антиген обнаружен не был.
| Интервал между сменой фаз, сутки | Титр антигена | ||||||
| Объем фазы, мл | I опыт | II опыт | III опыт | ||||
| Исходная фаза | Концентри- рованная фаза * | Исходная фаза | Концентри- рованная фаза * | Исходная
фаза | Концентри- рованная фаза * | ||
| 1 | 30 | 1 : 2 | 1 : 2 | ||||
| 3 | 30 | Исх. (±) | Исх. (±) | – | |||
| 3 | 30 | Исх. (±) | 1 : 4 | – | 1 : 4 | 1 : 4 | |
| 0 | 30 | – | – | – | – | ||
| (Промывные жидкости) | |||||||
| 4 | 30 | Исх. | 1 : 4 | Исх. | 1 : 4 | Исх. | 1 : 4 |
| 3 | 30 | Исх. (±) | Исх. (±) | Исх. | 1 : 8 | ||
| 4 | 30 | Исх. | Исх. | – | 1 : 2 | ||
| 2 | 30 | – | Исх. | – | 1 : 2 | – | Исх. |
| 5 | 30 | – | Исх. | – | 1 : 2 | ||
* Фазу концентрировали в 7–8 раз.
Необходимо отметить также, что в культурах гепатомы XXIIа происходило одновременно и накопление мышиного сывороточного альбумина.
Совокупность приведенных данных свидетельствует об образовании эмбрионального α-глобулина самими клетками гепатомы.
В предыдущих работах по изучению антигенной структуры мышиных гепатом в одном из штаммов был обнаружен антиген, отсутствующий в крови, печени и других органах нормальных взрослых мышей. Этот антиген был описан нами как специфический антиген гепатомы [11; 12; 17; 18]. В дальнейшем, однако, такой же антиген был обнаружен в эмбриональной мышиной сыворотке. В настоящей работе представлены данные об идентичности эмбрионального α-глобулина и антигена, вырабатываемого гепатомой, и получены доказательства о синтезе этого антигена самой опухолью. Очевидно, что в данном случае в гепатоме произошла своеобразная «дерепрессия» системы синтеза эмбрионального α-глобулина, находящейся в неактивном состоянии в тканях взрослого животного.
Прежде чем изучать биохимический механизм регуляции синтеза эмбрионального α-глобулина, необходимо возможно более точно выяснить ряд обстоятельств, связанных с его образованием в нормальной и малигнизированной ткани.
В какой ткани эмбриона синтезируется этот компонент? Хотя у нас нет прямых данных, все же наиболее вероятным представляется, что образование этого α-глобулина происходит в печени эмбриона. Действительно, показано, что эмбриональный α-глобулин синтезируется клетками гепатомы XXIIа и что его появление сопровождает только рост опухолей, возникших из печеночной ткани.
Если образование этого α-глобулина имеет место только в клетках, возникших из печеночной ткани, то надо думать, что и в нормальных условиях печеночная ткань является местом его синтеза. При этом следует подчеркнуть, что гепатомы, при росте которых обнаруживался эмбриональный α-глобулин, произошли из клеток печеночной паренхимы [7–9]. Они сохранили некоторые органоспецифические антигены этих клеток [9], а гепатома XXIIа при культивировании in vitro образовывала не только специфический α-глобулин, но и сывороточный альбумин – белок, синтезируемый клетками печеночной паренхимы. Таким образом, наиболее вероятным местом образования эмбрионального α-глобулина можно считать клетки печеночной паренхимы.
Что является решающим фактором в печеночной клетке, приводящим к «репрессии», а затем к активации синтезирующего механизма? Синтез изучаемого компонента прекращается во взрослом организме, когда клетки печени практически не делятся. Продукция α-глобулина возобновляется при регенерации печени и в клетках гепатом. Наибольшее накопление антигена сопровождает рост гепатомы XXIIа, обладающей самой высокой скоростью роста. На основании этих данных можно предположить, что образование эмбрионального α-глобулина может иметь место только в делящихся клетках печени и что переход печеночной клетки от покоя к делению является определяющим условием возобновления синтеза этого компонента. Подавление синтеза, наступающее во взрослом организме, не является необратимым, так как этот процесс вновь возобновляется при регенерации взрослой печени и в опухолевых клетках, возникших из печени взрослого животного.
Предположение о клеточном делении как решающем условии для активации системы, синтезирующей эмбриональный α-глобулин, допускает экспериментальную проверку. Можно проверить, имеется ли зависимость между числом митозов в печени и гепатомах и продукцией α-глобулина. Можно попытаться приостановить рост гепатомы в культуре и определить, будет ли при этом синтезироваться α-глобулин.
Возникает вопрос, не является ли эмбриональный α-глобулин белком митотического аппарата клетки. Нам кажется, что имеющиеся материалы позволяют ответить отрицательно на этот вопрос. Во-первых, он не образуется при росте даже таких быстро растущих опухолей, как карцинома Эрлиха или саркома Крокера. Во-вторых, соотношение концентраций изучаемого α-глобулина в сыворотке и в клетках опухолевой или регенерирующей ткани печени говорит в пользу того, что этот компонент является внеклеточным белком и, по-видимому, секретируется клеткой сразу же после его образования. Вероятнее всего, он выполняет какую-то функцию как сывороточный белок.
Обнаруженный феномен – синтез эмбрионального α-глобулина клетками гепатом – имеет, по-видимому, довольно широкое распространение. Так, например, совершенно аналогичное явление было обнаружено нами у крыс с гепатомой Зайдела. В сыворотке крысиных эмбрионов и новорожденных крысят обнаруживался α-глобулин с подвижностью, близкой к подвижности мышиного эмбрионального α-глобулина. В крови взрослых крыс этот компонент не выявлялся. Он вновь обнаруживался в асцитной жидкости крыс, привитых быстрорастущей асцитной гепатомой Зайдела, и не появлялся у крыс, привитых саркомой М-1.
Было бы крайне интересно выяснить, не аналогичен ли эмбриональный α-глобулин фетуину телят [19] и не будет ли образовываться фетуин при регенерации печени взрослых животных.
Для дальнейшего изучения вопроса о регуляции синтеза эмбрионального α-глобулина необходимо установить, не имеется ли корреляции между его исчезновением в онтогенезе и появлением в сыворотке а-глобулинов, свойственных взрослому животному [20; 21], а также не является ли его исчезновение в онтогенезе следствием изменения антигенной специфичности этого белка, а не прекращения его синтеза [21]. Поскольку для определения эмбрионального α-глобулина использовалась его антигенная специфичность, это предположение вполне допустимо. Однако отсутствие антител к изучавшемуся антигену в анти-ВМ-сыворотках говорит об отсутствии в сыворотке взрослых животных белков, даже частично родственных изучавшемуся α-глобулину.
Представляло бы большой интерес воспроизвести синтез описанного α-глобулина в бесклеточной системе и изучить вопросы регуляции его синтеза на молекулярном уровне.
В заключение мы хотели бы подчеркнуть особые преимущества иммунохимических методов, позволяющих не только следить за динамикой индивидуального антигена, находящегося в сложной смеси с другими белками, но и выделять его из этой смеси.
В сыворотке мышиных эмбрионов и мышей в ранний постнатальный период обнаружен антигенно-активный α-глобулин, отсутствующий в крови взрослых животных. Этот же антиген вырабатывается клетками перевиваемой гепатомы при росте ее на мышах, на крысах и в культуре ткани.
Поступила в редакцию 17. IX. 1962
G. I. ABELEV, S. D. PEROVA, N. I. KHRAMKOVA, Z. A. POSTNIKOVA and I. S. IRLIN
Institute of Epidemiology and Microbiology, Academy of Medical Sciences of the USSR, Moscow
In serum of mouse embryos and of mice in early postnatal period antigenically active α-globulin absent in blood of adult animals has been detected. This antigen is also produced by cells of transplantable hepatoma when grown on mice, rats and in tissue culture.