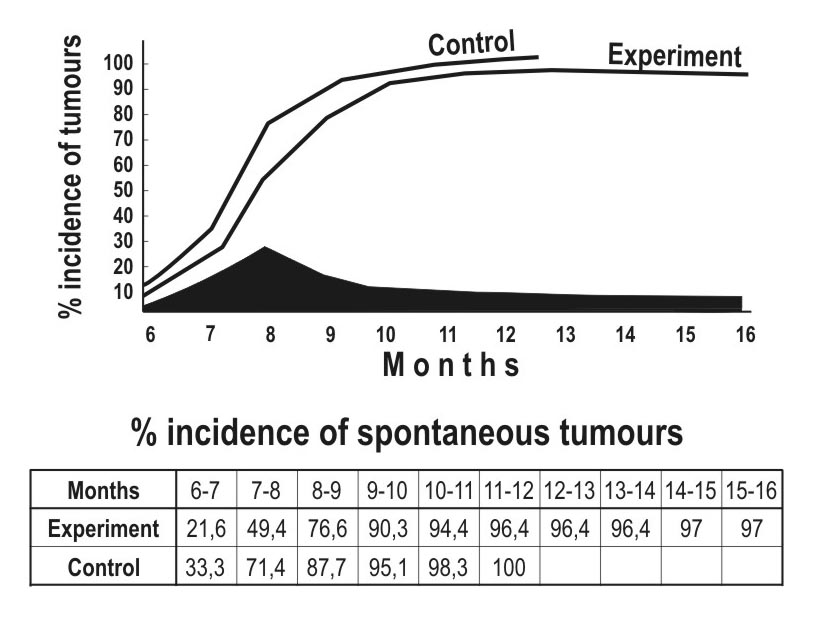
В аналогичных опытах Гирша (Hirsch, 1962) наблюдалась стимуляция опухолеобразования, что по мнению автора свидетельствует также об иммунологической природе феномена. Хорошо известно, что стимуляция или подавление роста опухолей в результате иммунизации определяется тем, включились ли в действие преимущественно клеточные или гуморальные факторы иммунитета.
Весьма ярким случаем иммунологического торможения вирусного канцерогенеза является подавление возникновения опухолей у взрослых хомяков, зараженных в новорожденном состоянии вирусом (Дейчман, Ключарева, 1965). Возникновение опухолей предотвращались введением вируса даже в конце латентного периода.
Значение иммунологических отношений опухоли и хозяина демонстрируется также тем фактом, что тимэктомия способствует вирусному и химическому канцерогенезу (Miller, 1964 и др.).
Роль этих отношений может быть особенно велика при вирусном канцерогенезе в условиях, когда онкогенный вирус действует не в естественном хозяине. Так, например, вирус куриной саркомы Рауса вызывает кисты и злокачественные опухоли у крыс. По данным Ирлина и Тер-Григорова (1965), из нашей лаборатории, у тимэктомированных сразу после рождения крыс в результате заражения вирусом Рауса резко уменьшается кистообразование, но образуются саркомы.
Таким образом, в этом случае изменение иммунологического статуса организма определяет конечный результат действия вируса — кисто- или опухолеобразование.
Неонатальная тимэктомия у кроликов, зараженных вирусом Рауса, резко усиливает злокачественность возникающих опухолей и у мышей значительно стимулирует индукцию полиомных опухолей.
Наличие иммунологических барьеров при вирусном канцерогенезе может служить фактором, определяющим частоту спонтанного возникновения некоторых опухолей. Так, например, Wahren (1966) показала, что линия AKR, характеризующаяся высокой частотой «спонтанных» лейкозов Гросса, толерантна по отношению к специфическому антигену этих опухолей.
Некоторыми наблюдениями установлена более выраженная антигенность по отношению к хозяину опухолей, индуцированных вирусами (полиома, SV 40, мышиные лейкозы) и химическими канцерогенами по сравнению со спонтанными опухолями (см. Syögren, 1965, Old, Boyse, 1964). Ряд данных позволяет думать, что дело здесь не столько в этиологическом агенте, сколько в иммунологических отношениях опухоли и хозяина. Было показано, что степень антигенности опухоли находится в обратной зависимости от длительности латентного периода при ее индукции (Old et al., 1962). Вместе с тем показано, что длительно развивающиеся трансплантаты сильно антигенной опухоли, вызванной SV 40, могут утрачивать свою антигенность (Дейчман и Ключарева, 1965). На основании этих наблюдений можно предположить, что большинство опухолей, индуцированных вирусами и канцерогенами, преодолевают иммунологические барьеры, в то время как длительно развивающиеся спонтанные опухоли обходят эти барьеры посредством селекции низкоантигенных вариантов или даже утраты специфических антигенов.
Все эти и многие другие данные указывают на несомненное наличие иммунологических взаимоотношений между опухолью и организмом хозяина.
При исследовании этих взаимоотношений используются различные методы.
Наиболее адекватным методом исследования противоопухолевого иммунитета является трансплантационный тест (см. Syögren, 1965). Однако его громоздкость, малая «разрешающая способность» и неколичественность заставляют искать серологические тесты противоопухолевого иммунитета. При саркомах и карциномах — противоопухолевый иммунитет обусловлен клеточными факторами и антитела при нем не были обнаружены. Только при экспериментальных лейкозах были найдены цитотоксические антитела.
Однако недавно (Лежнева, Зильбер, Иевлева, 1965) с помощью метода Кунса, с использованием живых опухолевых клеток, было показано, что в сыворотках мышей, иммунизированных изологичными канцерогенными саркомами, обнаруживаются специфические противоопухолевые антитела.
То, что эти антитела являются не просто «свидетелями» противоопухолевого иммунитета, но оказывают влияние и на рост опухоли, говорят опыты Möller (1964), а также опыты нашей лаборатории (Зильбер, Постникова) об эффекте стимуляции роста опухоли под влиянием специфических противоопухолевых сывороток или иммунизации. При иммунизации различными фракциями опухолевого экстракта наблюдался весьма четко выраженный эффект стимуляции.
Приведенные данные позволяют надеяться, что серологические подходы окажутся применимыми к исследованию противоопухолевого иммунитета и антигенов, его вызывающих.
Большое количество исследований по изучению иммунологии рака проведено с помощью гетерогенных сывороток.
Сложность антигенной структуры опухолей создает громадные трудности при их исследовании с помощью гетероиммунных сывороток. Именно поэтому наиболее убедительные данные по антигенной специфичности опухолей и противоопухолевому иммунитету были получены при использовании изологичных (сингенных) систем. Однако даже в тех случаях, когда возможен серологический анализ в сингенной системе, он не позволяет проведения столь тонких исследований, какие проводятся с гетеросистемами. Применение большинства иммунохимических тестов, включая иммунодиффузионный анализ, требует, как правило, гетероимунных сывороток. В настоящее время крайне важно найти подход, который позволил бы объединить данные анализа, проводимого с помощью изо- и гетерологичных сывороток. Как нам кажется, одним из подобных подходов может служить исследование антигенной структуры клеточных поверхностей. Как указывалось выше, метод флюоресцирующих антител позволяет обнаружить специфические противоопухолевые антитела в сингенной системе. Эти антитела локализуются на клеточной поверхности. Трансплантационный тест тоже, хотя и косвенно, свидетельствует о поверхностной локализации опухолевых антигенов.
Следовательно, поиски путей к антигенному анализу клеточной поверхности с помощью гетероиммунных сывороток могли бы дать новые возможности исследования специфических антигенов, ответственных за противоопухолевый иммунитет. Haughton (1962) показал, что нерастворимая фракция клетки — «клеточные тени» содержат антигены наружной мембраны клеток и что антитела к ним вызывают агглютинацию клеток. Белошапкина и Абелев (1965) в нашей лаборатории, получив антитела к «теням» клеток печени, показали иммуногистохимически, что эти антитела избирательно реагируют с наружной клеточной мембраной.
Белошапкина и Храмкова (1966) показали далее, что с помощью анти-теневых антител можно обнаружить органоспецифические антигены поверхностей печеночной клетки. Точно таким же методом можно получить и антитела к поверхностным антигенам асцитной гепатомы, хотя найти специфический антиген с их помощью пока не удалось (Белошапкина и Мендис, 1965).
Таким образом, эти опыты создают экспериментальный подход к анализу клеточных поверхностей с помощью гетероиммунных сывороток. Можно надеяться, что применение подобного подхода на таких моделях, как экспериментальные лейкозы, позволит ближе подойти к определению природы специфических опухолевых антигенов.
Иммунохимические подходы к изучению опухолей весьма многообразны. Но мы хотели бы остановиться еще лишь на одном феномене, изучаемом, главным образом, с помощью гетероиммунных сывороток. Речь идет о «дерепрессии» в опухолевых клетках синтеза антигенов, характерных для гемологичных эмбриональных клеток. О сходстве опухолевых и эмбриональных тканей имелись указания еще в работах Гиршфельда и последующих авторов (см. Вязов, 1962, Day, 1965), однако четкие доказательства этого явления были получены сравнительно недавно.
В 1963 г. Абелев и сотр. у нас в лаборатории показали, что клетки мышиных и крысиных гепатом продуцируют сывороточный α-глобулин, являющийся специфическим продуктом эмбриональных клеток печени. Продукция эмбрионального α-глобулина наблюдалась в различных штаммах перевиваемых и в некоторых первичных гепатомах. [ Абелев Г. И., Перова С. Д., Храмкова Н. И., Постникова З. А., Ирлин И. С. Эмбриональный сывороточный α-глобулин и его синтез перевиваемыми гепатомами мышей (1963) • Abelev G. I., Perova S. D., Khramkova N. I., Postnikova Z. A., Irlin I. S. Production of embryonal a-globulin by transplantable mouse hepatomas (1963) ] Феномен имеет общее значение для гепатом. Так Грабар и сотр. (1966) недавно подтвердили и значительно расширили эти наблюдения на крысиных гепатомах. Татаринов (1964) показал, что те же отношения имеют место при гепатоцеллюлярных раках человека. По-видимому, появление в опухолях эмбриональных антигенов свойственно не только гепатомам. Gold и Freedman (1965) четко показали, что в опухолях желудочно-кишечного тракта людей появляется антиген, отсутствующий в тканях кишечника взрослых, но характерный для эпителия кишки плода.
Своеобразная «дерепрессия» антигенов была обнаружена Old и Boyse (1964) в мышиных лейкозах. Ими было показано, что антиген строго специфический для тимоцитов некоторых линий мышей проявляется в лейкемических клетках мышей, имеющих или не имеющих этот антиген в тимусе. И здесь имеет место синтез антигена, характерного для незрелых клеток в опухолях лимфоидной ткани.
Таким образом, все эти наблюдения говорят о наличии какого-то общего механизма «дерепрессии», проявляющегося в злокачественных клетках.
Независимо от теоретического значения этого феномена, он начинает находить уже клиническое применение.
Появление эмбрионального α-глобулина в сыворотках больных первичным раком печени было использовано Татариновым (1964) как диагностический тест для отличия первичных и вторичных опухолей печени. Материал еще невелик, но и в нашей лаборатории совместно с клиническим отделением ИЭКО АМН СССР, С. Д. Перовой и И. В. Ассекритовой были получены обнадеживающие данные.
Указанными данными и направлениями отнюдь не исчерпываются возможности иммунологии в онкологических исследованиях, но и они иллюстрируют многообразие путей и плодотворных подходов в этой области.
Современная иммунология рака вплотную подошла к клинике. От координированной работы клиницистов и иммунологов зависит дальнейший прогресс этой области знания и возможность практического использования экспериментальных данных.

Творческий путь выдающегося ученого (о Л. А. Зильбере, 1971)
Л. А. Зильбер – иммунолог, вирусолог, онколог. К 90-летию со дня рождения
Г. И. Абелев, И. Н. Крюкова. Роль Льва Александровича Зильбера
в становлении современной вирусологии и иммунологии рака (1984)
Остался в своих учениках... К биографии Льва Александровича Зильбера (1989)
Школа Льва Александровича Зильбера в вирусологии и иммунологии рака (1990)
Школа Л. А. Зильбера (1994)